哈工大生命科學(xué)和醫學(xué)學(xué)部賀強、吳英傑教授團隊開(kāi)發(fā)出一種(zhǒng)遊動納米機器人用于ATP合成(chéng)及定向(xiàng)運輸
哈工大全媒體(劉培香 吳英傑 文/圖)近日,我校生命科學(xué)和醫學(xué)學(xué)部賀強、吳英傑教授團隊在仿生遊動納米機器人領域取得重要研究進(jìn)展,研究成(chéng)果以《旋轉FoF1-ATP合酶驅動的瓶狀戊聚糖膠體馬達用于ATP合成(chéng)和儲存》(Rotary FoF1‑ATP Synthase-Driven Flasklike Pentosan Colloidal Motors with ATP Synthesis and Storage)爲題,發(fā)表在《美國(guó)化學(xué)會(huì)志》(Journal of the American Chemical Society)上。該研究以納米尺度的旋轉生物分子馬達ATP合酶作爲動力部件,成(chéng)功實現了亞微米尺度遊動納米機器人仿生體系的生物能(néng)量貨币ATP合成(chéng)、儲存及定向(xiàng)運輸,該研究在主動靶向(xiàng)能(néng)量代謝調控治療等生物醫學(xué)領域具有廣闊的應用前景。
在生物體中,定向(xiàng)遷移和生物能(néng)量貨币ATP的供應對(duì)許多生理和病理過(guò)程至關重要。科學(xué)家們開(kāi)發(fā)了各種(zhǒng)具備正向(xiàng)或負向(xiàng)趨化能(néng)力的酶驅動遊動納米機器人以執行各種(zhǒng)生物醫學(xué)任務。然而,基于天然生物酶供能(néng)的遊動納米機器人對(duì)周圍的離子環境敏感,存在生理條件下難以實現高效驅動的實際問題。FoF1-ATP合酶作爲自然界最小的旋轉生物分子馬達,具有高效、安全的能(néng)量轉化優勢,且在生理條件下運轉良好(hǎo)。因此,開(kāi)發(fā)基于FoF1-ATP合酶作爲動力單元的遊動納米機器人仿生體系,完善其生理條件下的自驅動性能(néng)及生物醫學(xué)應用功能(néng),將(jiāng)爲遊動納米機器人執行精準診療任務提供重要的理論基礎。
該研究團隊以FoF1-ATP合酶作爲動力單元,成(chéng)功制備了一種(zhǒng)流線型、亞微米尺度的瓶狀遊動納米機器人。實驗數據分析和理論模拟表明,基于FoF1-ATP合酶的優勢和功能(néng),外部質子通過(guò)瓶徑向(xiàng)瓶腔内擴散協同驅動FoF1-ATP合酶發(fā)生磷酸化反應,能(néng)夠利用生物體内廣泛存在的ADP和無機磷酸鹽(Pi)合成(chéng)生物能(néng)源ATP,實現了生物安全的能(néng)量轉換和自主運動能(néng)力,同時(shí)展示出較高的ATP的合成(chéng)和儲存能(néng)力。在外部質子梯度的環境下,遊動納米機器人表現出明顯的負趨化性仿生行爲,即朝著(zhe)遠離質子源的方向(xiàng)沿質子梯度定向(xiàng)遷移。此外,當外部介質存在誘導ATP釋放的化學(xué)信号時(shí),遊動納米機器人能(néng)夠將(jiāng)内部儲存的ATP按需釋放。這(zhè)種(zhǒng)集ATP合成(chéng)、儲存和靶向(xiàng)遞送功能(néng)于一體的遊動納米機器人,爲與ATP失衡相關的疾病的精準治療提供了新思路。
生命科學(xué)和醫學(xué)學(xué)部賀強教授、吳英傑教授爲論文通訊作者,博士研究生李月爲論文第一作者,博士研究生劉君參與相關研究工作。
本研究獲得國(guó)家自然科學(xué)基金重大項目和國(guó)家重點研發(fā)課題的支持。
全文鏈接:https://pubs.acs.org/doi/full/10.1021/jacs.4c00334
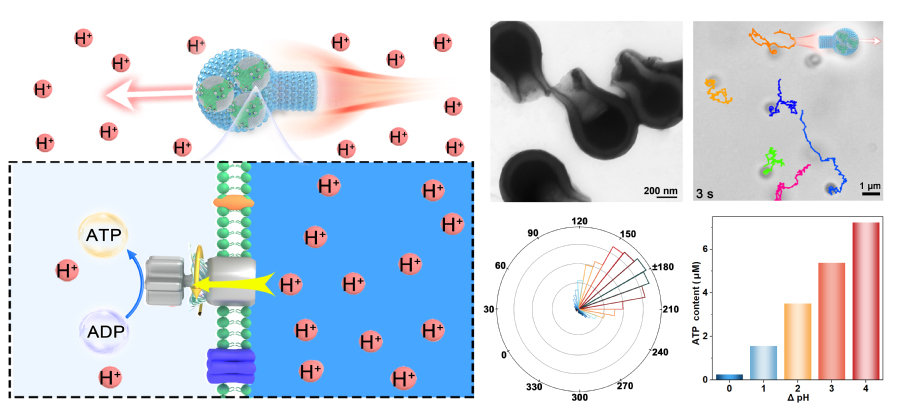
FoF1-ATP合酶分子馬達協同驅動的遊動納米機器人用于ATP合成(chéng)及定向(xiàng)運輸